
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Il kit di trasporto virus di BABIO ottiene l'autorizzazione FDA 510(k).
Il kit di trasporto virus di BABIO ottiene l'autorizzazione FDA 510(k).
Jinan, Cina – ottobre 2025— BABIO Biotechnology, un rinomato produttore cinese di reagenti diagnostici medici, annuncia con orgoglio che il suoKit di trasporto virus (non inattivante)ha ricevutoAutorizzazione FDA 510(k) (K250205), convalidando ufficialmente la sua conformità agli standard normativi statunitensi.
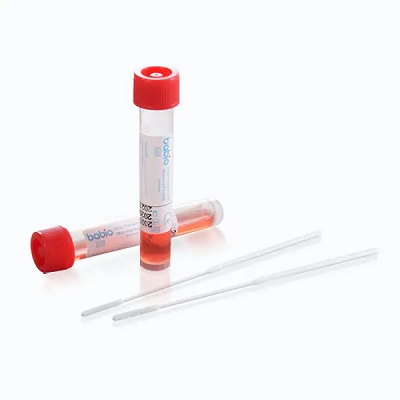
Questa pietra miliare rafforza la leadership globale di BABIO nelle soluzioni di trasporto di campioni clinici. Il kit è progettato per la raccolta sicura e stabile di campioni virali, supportando applicazioni a valle comeRT-PCR, cultura virale, Ediagnostica molecolare. È dotato di:
-
✅ Stabilità della temperatura ambiente
-
✅ Soluzione di Hank migliorata con antibiotici
-
✅ Provette coniche prive di DNasi/RNasi
-
✅ Tamponi floccati sicuri con design breakpoint
Disponibile in più volumi di riempimento (1 ml–6 ml) e confezioni (20–500 provette), il kit è ideale per ospedali, laboratori e istituzioni sanitarie pubbliche in tutto il mondo.
Con acapacità produttiva giornaliera di 100.000 unità, BABIO garantisce un'offerta costante e prezzi competitivi. Affidati aStati Uniti, Germania, e oltre, BABIO continua a fornire innovazione e affidabilità nei sistemi di trasporto dei virus. Ulteriori informazioni su https://www.babiocorp.com.
#VirusTransportKit #FDA510k #BABIO #ClinicalDiagnostics #VTM #RT-PCR #GlobalHealthcare #MedicalDevices #SpecimenCollection


